11-1. 강산에 의한 강염기의 적정
11-2. 강염기에 의한 약산의 적정
11-3. 강산에 의한 약염기의 적정
11-4. 이양성자성 계에서의 적정
11-5. pH 전극에 의한 종말점 검출
11-6. 지시약에 의한 종말점 검출
11-7. 실제적인 주의점
11-8. Kjeldahl 질소 분석법
11-9. 평준화 효과
11-10. 스프레드시트에 의한 적정 곡선의 계산
11-7. 실제적인 주의점
일차 표준 물질(primary standard)
: 순도가 높고 용액을 만들었을 시 무게 오차가 적어 예상한 농도와 거의 동일한 농도의 용액을 만들 수 있는 물질
일차 표준 물질(primary standard)로 사용할 수 있을 정도로 순수하게 얻을 수 있는 산과 염기들은 표 11-4에 수록
- NaOH와 KOH는 시약급 물질이 탄산 이온(대시 중 CO2와 반응한 결과)과 흡수한 물을 포함하기 때문에 일차 표준 물질이 될 수 없음
- NaOH와 KOH 용액은 일차 표준 시약으로 표준화해야 함
- 프탈산 수소 포타슘(KHP)은 이러한 목적으로 사용되는 가장 편리한 화합물 중의 하나
- 적정에 사용되는 묽은 NaOH 용액은 50 wt% NaOH 수용액으로 된 저장 용액을 묽혀서 제조함
- 저장 용액 속의 탄산 소듐은 비교적 불용성이며 밑으로 가라앉음
- 염기성 용액(0.1 M NaOH)은 대기와 차단되어야 하는데, 그렇지 않으면 CO2를 흡수함
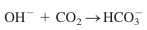
- 표준 용액은 일반적으로 돌려 닫는 뚜껑을 이용하는 고밀도 폴리에틸렌 용기에 보관해야 하며, 병 속에서 증발되는 과정을 통해 시약의 농도는 서서히 변화함
- 알루미나 백에 용기를 넣어 밀폐시킬 경우 10배 정도 증발을 줄일 수 있음
- 표준 용액은 일정한 보관 수명이 있다는 것
- 강염기성 용액은 유리를 부식시키므로 플라스틱 용기에 보관하는 것이 가장 좋음
- 이 용액은 필요 이상으로 뷰렛에 오래 보관하지 않음
- 플라스크 내에서 0.01 M NaOH를 1시간 동안 가열하면 NaOH의 몰농도가 10% 감소하는데, 이는 OH-와 유리가 반응하기 때문임
Keyword: 일차 표준 물질(primary stnadard)



